Introduction
Je fais ma thèse au Centre d’Océanologie de Marseille et à l’Ecole Nationale Supérieure de Chimie de Paris. Je vais vous parler de "mémoire" puisque je vais vous expliquer comment la Terre peut garder "en mémoire" des informations sur son passé. Je travaille sur un lac, le lac Masoko (photo 1). Ce lac est situé dans le Sud-Ouest de la Tanzanie dans une chaîne de montagnes, la chaîne du Rungwe. La carte présentée figure 1 situe le lac Masoko dans la zone frontalière avec le Malawi. Cette zone correspond à la zone des grands lacs du Rift africain avec au Nord-Ouest le lac Tanganyika et au Sud-Est le lac Malawi (lac Nyassa pour les Tanzaniens). Ces lacs font plusieurs dizaines de milliers de kilomètres carrés. En comparaison, le lac Masoko est tout petit : il fait environ 700 mètres de diamètre. C’est un lac de cratère volcanique. Le lac Masoko est un site d’étude particulièrement intéressant parce qu’il y a au fond du lac une sédimentation continue depuis 50 000 ans ce qui en fait un site d’étude privilégié pour étudier les variations du climat et des écosystèmes depuis 50 000 ans.

Photo Romain de Mesmay, mars 2006

D’où viennent les sédiments ?

Le sédiment c’est tout ce qui se dépose au fond d’un lac ou au fond d’un océan (figure 2). Les sédiments peuvent avoir de très nombreuses origines : des débris minéraux peuvent être apportés par les rivières, le vent peut déposer à la surface de l’eau des poussières qui finissent par tomber au fond... Quand les organismes meurent, leurs tissus se décomposent et une partie de la matière qui les constitue (la matière organique) peut sédimenter (tomber au fond de l’eau). On retrouve ainsi sur les fonds des débris provenant des organismes vivants dans l’eau (algues, bactéries...) ou des organismes vivant autour de l’écosystème considéré (végétaux terrestres, microorganismes du sol...). Enfin les activités humaines peuvent générer toutes sortes de déchets et de pollutions qui peuvent se retrouver dans les eaux et dans les sédiments. Chaque couche de sédiment se dépose sur les sédiments plus anciens. Contrairement aux historiens qui représentent souvent l’axe des temps horizontalement, l’échelle de temps des sédimentologistes et des paléoclimatologues est une échelle de temps verticale : plus on va profondément dans les sédiments et plus on remonte dans le temps.
Comment étudier les sédiments ?

Pour étudier les sédiments, on réalise un carottage. Cela consiste à enfoncer un tube dans le sédiment pour pouvoir remonter à la surface un cylindre de sédiment (figure 3). Le haut de la carotte correspond aux sédiments qui viennent d’être déposés : "le présent", le bas de la carotte correspond à la période la plus ancienne. La première chose à faire pour étudier une carotte de sédiment, c’est d’effectuer une datation. Certains sédiments présentent des couches annuelles que l’on peut observer à l’œil nu. Pour compter les années il suffit donc de compter les couches à partir de la surface du sédiment. C’est la méthode de datation la plus simple mais très peu de sédiments présentent ces couches annuelles. Certains évènements particuliers peuvent laisser des traces dans les sédiments. Par exemple, dans la carotte montrée en figure 3 sur laquelle je travaille actuellement, on trouve des cendres volcaniques provenant d’une éruption qui a eu lieu dans la région du Rungwe vers 1674 après J.C. ce qui permet de dater avec précision une des tranches de sédiments. Ce genre d’évènements n’est utilisable que pendant la période historique pendant laquelle des documents écrits peuvent permettre de dater les évènements.
La datation au carbone 14
C’est une méthode de datation qui est très utilisée en archéologie et qui peut être utilisée également pour dater des sédiments. Le carbone 14 (noté 14C) est un isotope radioactif du carbone (le carbone non radioactif est le carbone 12) qui a une durée de demi vie de 5730 ans. Cela signifie que le 14C perd la moitié de sa radioactivité au bout de 5730 ans. Le 14C est produit dans la haute atmosphère par la réaction suivante :
neutron + 14N → 14C + H
Un neutron réagit avec un atome d’azote (N) pour produire un atome de 14C et un atome d’hydrogène (H). Le 14C réagit ensuite avec l’oxygène pour former du dioxyde de carbone radioactif :
14C + O2 → 14CO2
Il y a très peu d’atomes de carbone radioactifs dans notre environnement : seulement 1 pour 1012 atomes de carbone 12 non radioactif. Le dioxyde de carbone (radioactif ou pas) peut être utilisé par les algues ou par les végétaux terrestres pour produire de la matière organique lors de la photosynthèse :
CO2 + H2O → Matière organique (C,H,O) + O2
C’est ainsi que tous les organismes vivants contiennent une faible quantité de carbone radioactif. Tant que les organismes restent vivants, il y a un équilibre qui s’établit entre le 14C qui se désintègre par radioactivité (14C → β- + 14N) et celui qui est absorbé par les organismes vivants. Leur concentration en carbone radioactif reste donc constante. En revanche, lorsque les organismes meurent, il n’y a plus d’apport en carbone et la désintégration radioactive du 14C entraîne une diminution de la teneur en 14C de la matière organique. La figure 4 montre le nombre de désintégrations par minute (l’activité radioactive) au cours du temps du 14C.

Les organismes vivants (y compris les humains !) possèdent une radioactivité due au carbone qui est de 13,6 désintégrations par minute. Lorsqu’un organisme meurt, la teneur en 14C de sa matière organique va diminuer. La connaissance de la courbe de décroissance radioactive du carbone permet, en mesurant la radioactivité, de connaître l’âge de la matière organique, c’est-à-dire de savoir quand l’organisme qui a produit cette matière organique est mort. Sur la courbe on voit que si la radioactivité mesurée est de 4 désintégrations par minute, alors l’age de la matière organique est d’environ 10 000 ans. L’unité de temps utilisée est appelée année BP pour l’anglais Before Present, c’est le nombre d’année avant la période actuelle. Il existe de très nombreuses autres méthodes de datation. Chaque méthode de datation possède sa propre précision et ses propres limites, la méthode de datation au carbone 14 ne permet pas de dater des objets plus anciens que 50 000 ans. Le choix de la méthode est tellement important que lorsque l’on donne un age on précise en général "age 14C" pour indiquer quelle est la méthode de datation.
Comment des êtres vivants peuvent "jouer avec le temps" ?
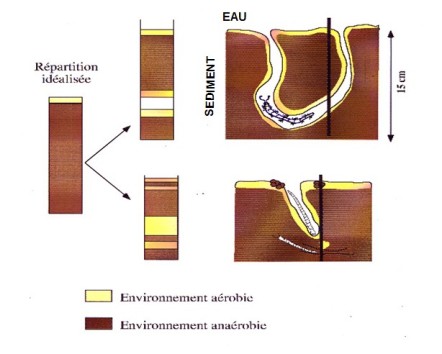
Il est très important, pour faire des études sur les carottes de sédiments, que les couches de sédiments se déposent bien horizontalement les unes à la suite des autres. Si la sédimentation n’est pas régulière ou s’il y a des mélanges de différentes couches de sédiments cela entraîne des problèmes dans les interprétations des études paléoenvironnementales. Il existe par exemple des organismes dits "bioturbateurs" qui vivent dans le sédiment et creusent des galeries, mélangeant différentes couches de sédiments (figure 5). Ces organismes peuvent ainsi enfouir une couche de sédiments récents sous une couche de sédiments plus anciens. Si on fait une étude à cet endroit là on ne trouvera pas comme d’habitude des sédiments plus vieux en dessous des sédiments plus récents. Le travail des géologues sur une carotte de sédiments, consiste à s’assurer que la sédimentation est continue et à décider pour quelles tranches les datations seront réalisées. On ne peut malheureusement pas dater toutes les tranches d’une carotte de sédiments, cela coûterait beaucoup trop cher.
Les biomarqueurs
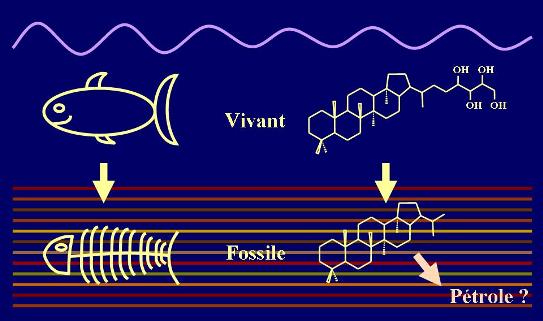
Un fossile d’organisme (de dinosaure, de poisson...) est une sorte d’empreinte de son squelette que l’on peut retrouver dans des sédiments plus ou moins anciens (figure 6). Il existe également des molécules fossiles. Voici une molécule qui est produite par les bactéries : le bactériohopanol (en haut à droite de la figure 6). Lorsque les bactéries meurent, leurs cellules vont se dégrader, se décomposer, et une partie des molécules qui composent ces cellules va pouvoir atteindre le sédiment après avoir subi des réactions chimiques ou biologiques. La matière organique peut être ingérée par d’autres organismes qui vont la digérer et donc la transformer. Dans le sédiment, on ne va pas toujours retrouver cette molécule intacte mais parfois elle aura été modifiée. A partir du bactériohopanol, on obtient une molécule, hopane (en bas à droite de la figure 6), qui est une molécule fossile ou biomarqueur. Elle a perdu une partie de la structure de départ : la partie contenant les fonctions alcools (-OH) dans le bactériohopanol, mais sa structure reste suffisamment caractéristique pour savoir qu’elle a été produite par des bactéries. Certaines molécules peuvent se retrouver intactes dans les sédiments, d’autres vont subir des transformations qui peuvent prendre plus ou moins de temps. Au bout de quelques millions d’années, certaines molécules issues du vivant peuvent se transformer en pétrole.
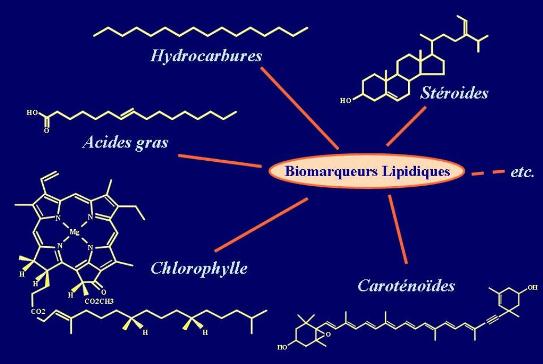
La figure 7 montre quelques exemples de l’incroyable variété de molécules que l’on peut trouver dans les sédiments. On s’intéresse principalement aux lipides parce qu’ils sont mieux conservés que les sucres et les protéines. Les hydrocarbures contiennent uniquement des atomes de carbone et d’hydrogène. Il ne faut pas penser que tous les hydrocarbures proviennent des activités humaines et de la pollution, il existe de très nombreux hydrocarbures qui sont produits par les plantes ou par les algues. Les acides gras sont des molécules que l’on trouve dans les parois des cellules. Leur structure varie en fonction des organismes qui les produisent. Voici deux exemples de pigments utilisés pour la photosynthèse (chlorophylle et caroténoïdes). Ces pigments sont des molécules très complexes et très fragiles. On les trouve intacts uniquement dans les sédiments récents, alors que dans les sédiments plus anciens on retrouve des composés issus de leur dégradation. Enfin les stéroïdes sont des biomarqueurs très intéressants parce qu’on les trouve dans de très nombreux organismes et que leur structure varie fortement d’une espèce à l’autre
Un exemple de biomarqueur : les alcénones
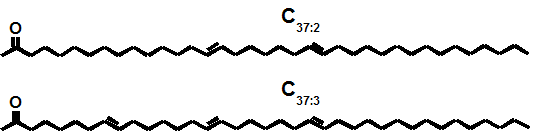
Les alcénones sont des molécules qui possèdent à la fois une double liaison C=O et des doubles liaisons C=C (figure 8). La notation C37 :2 signifie que la molécule contient 37 atomes de carbone et 2 doubles liaisons C=C. Le nombre de ces doubles liaisons est très important. Dans l’océan actuel, ces molécules sont produites deux espèces d’algues planctoniques : Emiliania huxleyi (voir photo 2) et Gephyrocapsa oceanica. Ces algues sont présentes dans presque tous les océans mais aussi dans certains lacs. Elles ont la particularité de produire les deux molécules C37 :2 et C37 :3 en concentrations différentes selon la température. Plus la température est élevée, plus la proportion de C37 :2 est importante. La production de ces 2 molécules en fonction de la température a d’abord été étudiée à partir de cultures pures d’algues effectuées à température contrôlée et dans lesquelles les concentrations de C37 :2 et C37 :3 ont été mesurées. Le rapport de concentration suivant a été établi :
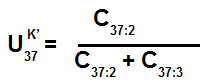

Une très bonne corrélation linéaire entre la température de culture des algues et la valeur obtenue pour le rapport UK’37 a été obtenue (courbe en pointillés sur la figure 9). La figure 9 montre les résultats de deux autres études qui ont eu lieu dans l’Atlantique et dans le Pacifique le long des cotes de l’Amérique du Sud. Lors de ces deux études, des prélèvements d’eau ont été réalisés en différents endroits et les alcénones produites par Emiliania huxleyi ont été analysées. En reportant les valeurs du rapport UK’37 en fonction de la température moyenne annuelle des eaux de surface on obtient également une droite qui est le signe d’une très bonne corrélation entre la température des eaux de surface et la mesure du rapport UK’37.
Comment déterminer les températures du passé ?
Les alcénones produites par les algues Emiliania huxleyi se conservent dans les sédiments. Si on mesure leur abondance et qu’on calcule le rapport UK’37, il est possible de déterminer la température des eaux de surface en utilisant la courbe d’étalonnage de la figure 9. La figure 10 montre un exemple d’étude des paléotempératures (températures du passé) en utilisant les alcénones. Une carotte de sédiments d’environ 10 m de longueur a été prélevée dans l’Océan Pacifique au large de l’Equateur par 2700 mètres de profondeur. Elle permet d’étudier les variations des températures depuis environ 150 000 ans. Les tranches de sédiments ont été analysées pour déterminer leur concentration en alcénones afin d’en déduire le rapport UK’37 puis la température des eaux de surface correspondante. Les sédiments de surface (la période "actuelle") montrent que la température des eaux est d’environ 24 °C alors qu’il y a environ 20 000 ans, la température était d’environ 21 °C. Cette époque correspond à la dernière période glaciaire. L’étude de ces biomarqueurs permet de reconstituer les variations de la température.


Quelles informations peuvent apporter les biomarqueurs ?
Il existe une très grande variété de structures de biomarqueurs ce qui permet d’obtenir des informations très variées sur les écosystèmes du présent et du passé. On peut avoir des informations sur l’origine de la matière organique pour savoir si celle-ci vient de l’activité biologique à l’intérieur du lac (algues, bactéries) ou bien de son environnement terrestre (végétaux).
Certaines molécules sont spécifiquement produites par une seule espèce d’organisme. Ceci est très intéressant car la détection de ces molécules dans un échantillon de sédiment permet de démontrer que l’espèce qui les a produites était présente à cet endroit là, à ce moment là. Voici quelques exemples de biomarqueurs spécifiquement produits par certaines algues :
- botryococcènes : Botryococcus braunii
- isoprénoides hautement ramifiés (HBI) : diatomées
- dinostérol : dinoflagellées
- alcénones : prymnesiophytes...
D’autres molécules vont fournir des informations sur les conditions environnementales : température, pH, conditions rédox, profondeur et oxygénation de la zone éclairée...
Conclusion
Pour étudier les écosystèmes du passé, il faut au préalable faire des études sur les environnements actuels pour faire un recensement des molécules et déterminer les organismes qui les produisent, ainsi que des cultures au laboratoire pour simplifier les problèmes et comprendre de quels processus dépendent les molécules que l’on trouve dans l’environnement. Ce n’est qu’une fois que l’on connaît bien la situation actuelle que l’on peut avoir des connaissances sur les environnements anciens.
-
Cf. Vincens, Annie, et al., "Pollen-based vegetation changes in southern Tanzania during the last 4200 years: climate change and/or human impact", in Palaeogeography, Palaeoclimatology, Palaeoecology, n°198, 2003, pp. 321-334. ↩
-
Gilbert, Franck, "Bioturbation et devenir de la matière organique", UE18 M1 Master d’Océanographie (COM - Université de la Méditerranée). ↩
-
Lichtfouse, Eric, in L’Actualité Chimique, n° 230, 2000, pp. 5-19. ↩
-
Grossi, Vincent, UMR 5125 PEPS, pers. comm. ↩
-
Prahl, Fredrick G, et al., "Alkenone paleothermometry: Biological lessons from marine sediment records off western South America", in Geochimica et Cosmochimica Acta, n° 70, 2006, pp. 101-117. ↩
